摘要:2025年欧洲肿瘤内科学会(ESMO)年会已于当地时间10月17至21日在德国柏林召开。本次年会中,哈尔滨医科大学附属肿瘤医院张清媛教授团队报告了III期BRIGHT-3研究预设中期结果,旨在探索吡洛西利联合来曲唑/阿那曲唑对......
2025年欧洲肿瘤内科学会(ESMO)年会已于当地时间10月17至21日在德国柏林召开。本次年会中,哈尔滨医科大学附属肿瘤医院张清媛教授团队报告了III期BRIGHT-3研究预设中期结果,旨在探索吡洛西利联合来曲唑/阿那曲唑对比安慰剂联合来曲唑/阿那曲唑治疗HR+/HER2-晚期乳腺癌的疗效和安全性(摘要号:490P)1。BRIGHT-3研究为吡洛西利在中国HR+/HER2-晚期乳腺癌中的应用提供了夯实的循证医学证据,更展现了我国在创新药物研发领域的重大突破,有望为患者带来新的治疗选择,改变临床实践。值此之际,医脉通特邀张清媛教授对该研究进行介绍、深入解读与点评。
CDK4/6抑制剂再添新证,吡洛西利为HR+/HER2-晚期乳腺癌患者带来新选择
BRIGHT-3研究是一项在中国58家中心开展的随机、双盲的III期临床试验。研究共纳入397例HR+/HER2−晚期乳腺癌患者,按2:1比例随机分为吡洛西利组(n=263)和安慰剂组(n=134),以28天为一周期口服给药。
吡洛西利组:吡洛西利360mg,BID+2.5mg来曲唑/1mg阿那曲唑,QD
安慰剂组:安慰剂+2.5mg来曲唑/1mg阿那曲唑,QD
主要研究终点为研究者评估的PFS,次要研究终点为盲态独立评审委员会(BICR)评估的PFS、总生存期(OS)、客观缓解率(ORR)、临床获益率(CBR)、疾病控制率(DCR)、缓解持续时间(DoR)和安全性。
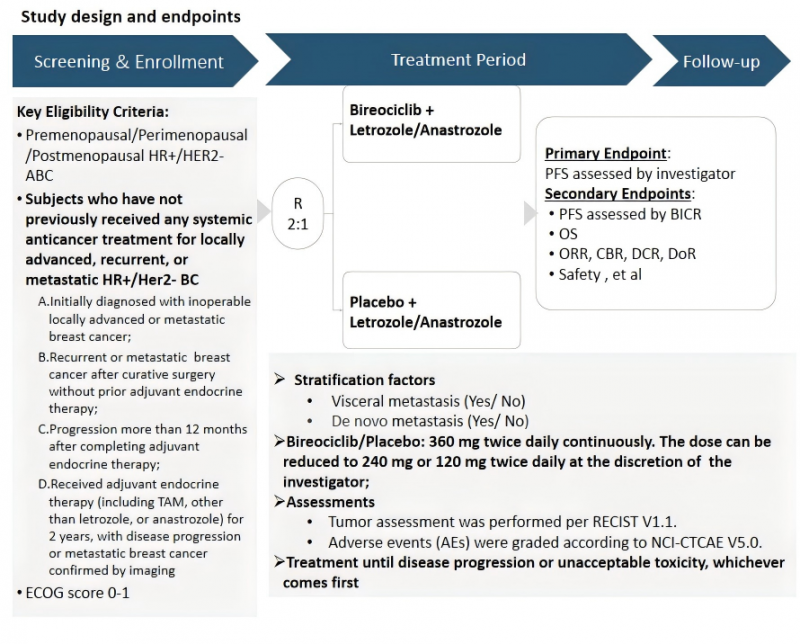
图1.研究设计及研究终点1
截至2025年1月10日,中位随访时间为20.7个月。意向治疗(ITT)人群中,55.7%的患者有内脏转移,41.3%有原发转移。此外,87.9%的患者未出现内分泌治疗耐药(包括A类、B类和C类人群,图1),12.1%的患者在接受至少2年的他莫昔芬/托瑞米芬辅助内分泌治疗后病情进展(D人群,图1)。
本次中期分析显示,吡洛西利组研究者评估的中位PFS(mPFS)未达到(NR)(95%CI:25.76-NR),安慰剂组为18.43个月(95%CI:14.75-21.36)(HR=0.53,95%CI:0.39-0.73,p<0.0001),疾病进展或死亡风险降低47%(图2A)。同时在吡洛西利组中,BICR评估的mPFS也为NR(95%CI:NR-NR),安慰剂组为19.55个月(95%CI:17.41-NR)(HR=0.51,95%CI:0.35-0.72,p<0.0001),与研究者评估结果一致(图2B)。
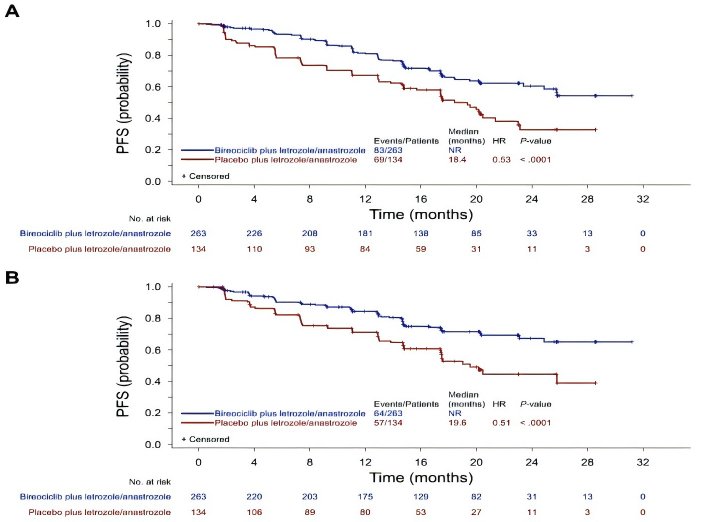
图2.ITT人群中研究者评估PFS(A)及BICR评估PFS(B)的Kaplan-Meier图1
在所有亚组中,吡洛西利均显示出mPFS获益,其中肝转移患者(HR=0.36,95%CI:0.19-0.68)、仅骨转移患者(HR=0.37,95%CI:0.06-2.23)、ER+/PR-患者(HR=0.37,95%CI:0.16-0.86)、经SERM类药物辅助治疗的继发性耐药患者(HR=0.39,95%CI:0.16-0.96)亚组获益最为显著(图3)。
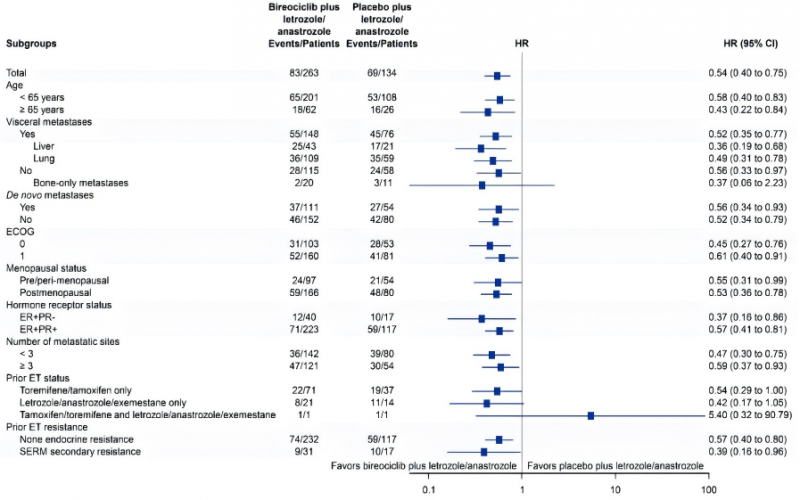
图3.ITT人群各亚组患者PFS分析1
吡洛西利次要研究终点数据亦取得亮眼成果:
ORR
· ITT人群:63.5%(95%CI:57.36-69.33) vs 42.5%(95%CI:34.04-51.37),p<0.0001;
· 伴有可测量病灶的患者:67.6%(95%CI:61.39-73.41) vs 43.8%(95%CI:35.16-52.82),p<0.0001。
中位DoR
24.2个月(95%CI:21.09-NR) vs 17.7个月(95%CI:13.90-NR)
OS
数据尚未成熟。
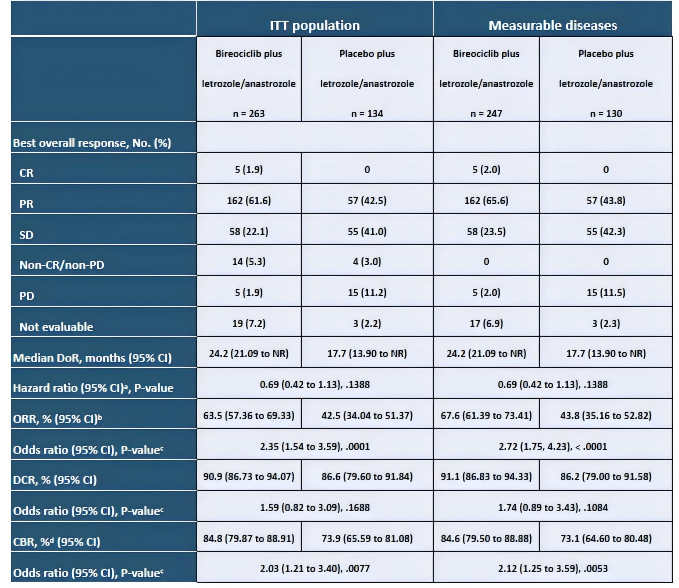
图4.研究者评估的ITT人群和伴有可测量病灶患者的肿瘤疗效1
安全性方面,吡洛西利组常见治疗期间不良事件(TEAE)为腹泻(93.5%)、中性粒细胞减少(78.7%)、白细胞减少(78.3%)和贫血(61.6%)。多数不良事件为1-2级,通常可以通过支持治疗和剂量调整进行有效管理。
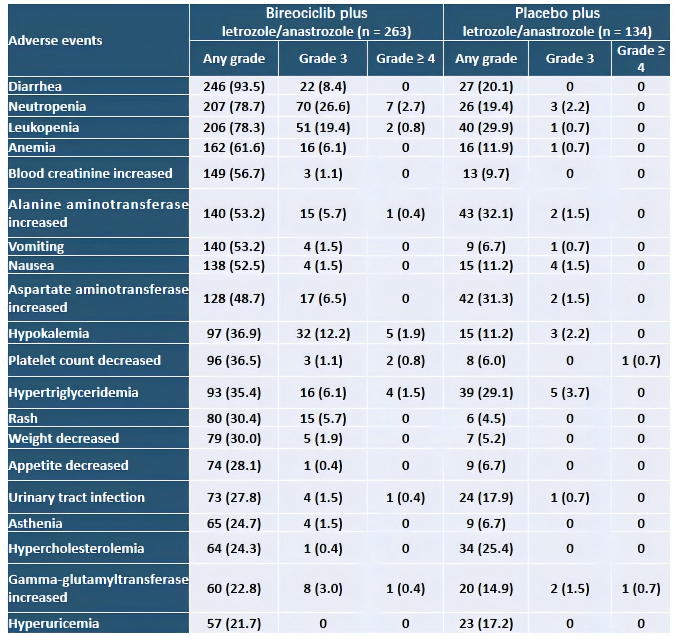
图5.发病率≥20%的TEAE1
专家点评
破局引领:吡洛西利为HR+/HER2-晚期乳腺癌治疗注入新动能
CDK4/6抑制剂联合内分泌治疗已成为HR+/HER2-晚期乳腺癌的一线标准方案。吡洛西利作为我国自主研发的新型高选择性CDK4/6抑制剂,不仅精准抑制CDK4/6,还兼具CDK2/CDK9附加抑制活性,从机制上具备差异化优势。II期BRIGHT-1研究2证实,难治性HR+/HER2-转移性乳腺癌患者持续单药剂量使用吡洛西利达到11.0个月的mPFS,ORR达29.8%,且毒性可控。随后,III期BRIGHT-2研究3显示,吡洛西利联合氟维司群显著改善了mPFS,较安慰剂组延长了7.36个月,并使肿瘤负担减少30.7%。这一系列研究成果不仅凸显了吡洛西利在晚期乳腺癌治疗中的重要价值,更展现了中国原研创新药物在国际肿瘤治疗领域的突破性进展。随着更多临床证据的积累,吡洛西利有望为HR+/HER2-晚期乳腺癌患者提供更有效、更安全的治疗选择,推动我国医药创新迈向全球领先水平。
双优答卷:吡洛西利实现全人群获益,疗效与安全并重
BRIGHT-3研究1的中期分析结果显示,吡洛西利联合来曲唑/阿那曲唑在ITT人群中mPFS显著延长,且在不同耐药背景、不同转移部位的患者中均观察到一致获益,凸显其优异的抗肿瘤活性优势。肝转移一直是HR+/HER2-晚期乳腺癌治疗的难点,患者预后普遍较差。本研究在肝转移亚组中观察到HR低至0.36的显著获益,mPFS延长近3倍,这一数据不仅与BRIGHT-1、BRIGHT-2系列研究2-3中吡洛西利在肝转移患者中的表现相互印证,也提示该药物在难治性病灶中仍能维持强效抑制能力。此外,在经SERM类药物治疗后继发耐药人群中,吡洛西利联合治疗亦展现出HR为0.39的显著优势,为mPFS超过20个月的长期疾病控制提供了可能,这为既往辅助治疗失败的患者带来了新的希望。该研究纳入多类人群进行分析,拓宽了CDK4/6抑制剂的适用边界,为中国患者提供了更为贴近临床实际的治疗选择。
同时,吡洛西利常见TEAE如腹泻、中性粒细胞减少等多为1-2级,安全性可管可控。并且吡洛西利作为口服制剂,相较于部分需静脉给药的传统方案,极大提升了用药便利性,有助于患者在长期维持治疗中保持依从性。尤其对于晚期患者而言,居家服药可减少频繁住院带来的身心负担,更符合“以患者为中心”的慢病化管理理念。
未来可期:吡洛西利引领乳腺癌治疗新标杆,点亮生命新希望
BRIGHT-3研究的中期成果标志着中国原研CDK4/6抑制剂在前线治疗领域的重大突破,展现了我国在抗肿瘤创新药物研发领域的强大实力。期待后续OS结果成熟以及真实世界证据的积累,吡洛西利有望成为中国HR+/HER2-晚期乳腺癌一线治疗的重要选择。其兼具疗效、安全性与用药便利性的特点,将进一步提升我国乳腺癌药物的可及性与可负担性,为更多患者带来优质的用药选择,提升生存获益,改善生活质量。未来,我们期待看到更多关于吡洛西利在前线治疗、联合策略及生物标志物探索方面的研究进展,以期为中国乳腺癌患者提供更加精准、个体化的治疗选择,推动我国乳腺癌诊疗水平提质增效。
